分子印迹是重要的仿生识别材料制备技术,分子印迹聚合物(MIP)作为重要的抗体模拟物,已经在分离、疾病诊断、药物递送、单细胞分析、生物成像和癌症诊疗等领域得到了广泛应用。国际上对MIP的分子识别性能的优化,主要是考虑分子印迹空腔的结构和性能。而实际上,分子印迹材料由印迹空腔和非印迹区域组成,其整体分子识别性能不仅由印迹空腔决定,还受到非印迹区域的影响。通常的分子印迹策略中,由于非印迹区域也是在与印迹空腔相同的聚合条件下形成的,因此,在"最优"条件下,在非印迹区域表面也存在着丰富的功能基团,能够产生明显的非特异性吸附,从而所得MIP无法同时具备最强的亲和力和最高的特异性,而只是这两者间的折中。
近日,我校生命分析化学国家重点实验室刘震教授团队报道了一种新颖的分子印迹和包覆(MIC)策略,有效地解决了上述长期困扰分子印迹技术的关键问题。该策略的原理如图1a所示,在印迹完成之后,再利用化学惰性的聚合试剂形成一层薄薄的包覆层去精准可控地覆盖非印迹区域,从而大大减少非印迹区域的非特异性吸附。基于此原理,该团队进一步提出了一个特殊的称为硼亲和锚定表位定向表面印迹和包层法(BOSIC)的MIC方法(图1b),所得包覆分子印迹聚合物(cMIP)的亲和力和特异性得到了显著提升。
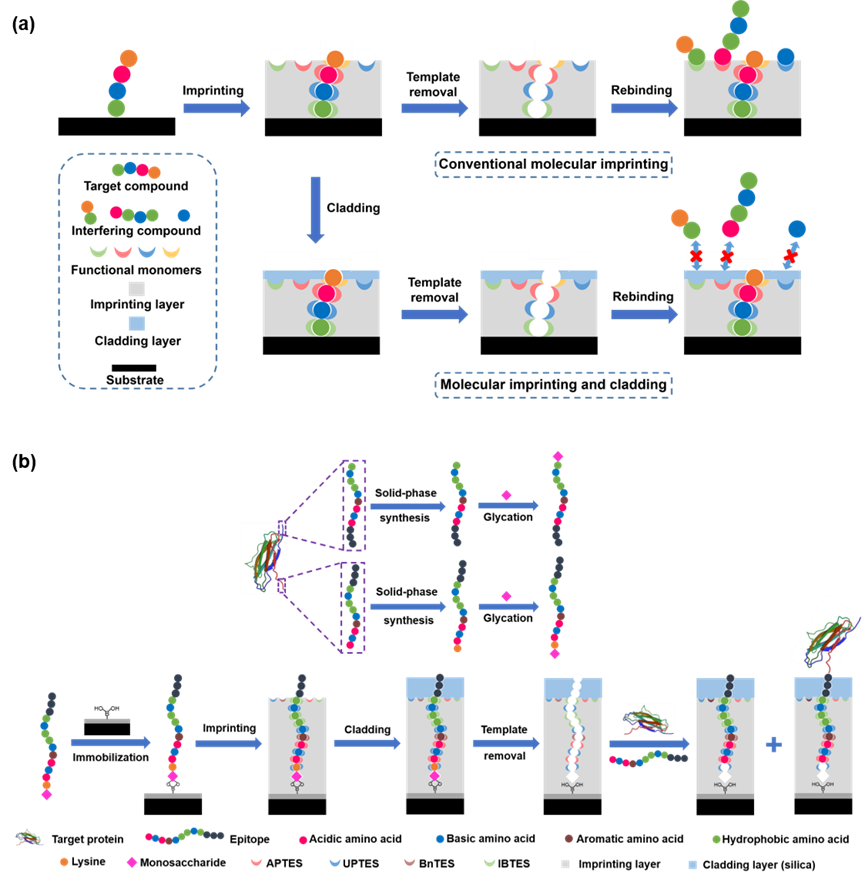
图1. (a)分子印迹和包覆策略的原理示意图,(b)硼亲和锚定表位定向表面印迹和包覆法的原理示意图
功能单体比例和印迹时间是两个最重要的印迹条件,主要根据印迹因子(IF)进行优化,其中IF为MIP与非印迹聚合物(NIP)结合模板量的比值。传统印迹方法制备的MIP和NIP的结合能力随着整体功能单体比例的增加而增加,MIP在第8个印迹条件(图2,紫心)达到最高,然而为了获得最高的IF值,避免较高的非特异性吸附,MIP只能牺牲结合能力,优化得到的印迹条件(图2a,蓝心)并非正真的最优,而实为伪最优。而MIC策略制备的cMIP虽然结合能力对单体比例的依赖性与MIP几乎相同,但是相应的cNIP在所有的单体比例下的结合能力均非常低,因此cMIP能够同时获得最高的结合能力和较低的非特异性吸附,IF值大大提高,优化得到的印迹条件(图2b,红心)是真正最优条件。MIC策略相比于传统印迹方法的优势在于:MIP在最强亲和力的印迹条件下(图3a,紫线)的特异性非常差(图4,紫框),而在伪最优印迹条件下,虽然特异性增高(图4,蓝框),但是亲和力大大减弱(图3a,蓝线),显然MIP的特异性增高是以牺牲亲和力为代价的;而cMIP在真正最优印迹条件下能够同时获得最强的亲和力(图3b,红线)和最高的特异性(图4,红框),已经在癌细胞靶向荧光成像(图5)和c肽分析(图6)中展现出显著优势。
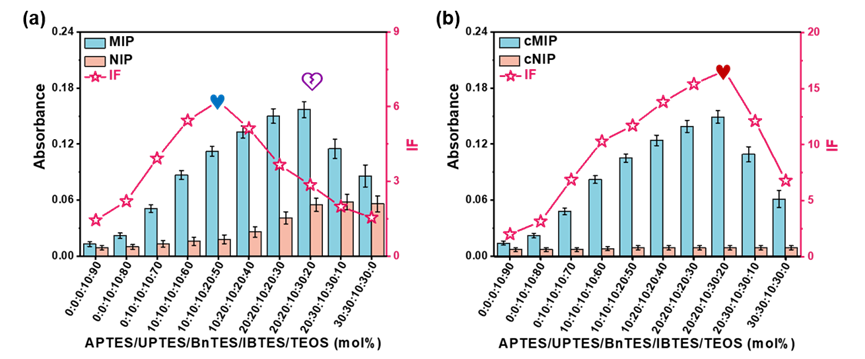
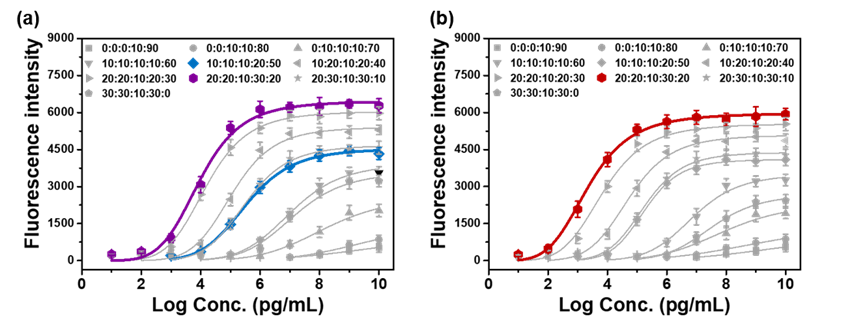
图2. 不同单体比例下制备的MIP和NIP(a)以及cMIP和cNIP(b)对测试化合物的吸光度 图3. 不同单体比例下制备的MIP(a)和cMIP(b)的吸附等温线

图4. 在肽段(a)和蛋白(b)水平的特异性考察


图5. 癌细胞荧光成像 图6. 基于双重cMIP的c肽分析
这一成果近期在Science Bulletin 上在线发表,刘震教授为论文的通讯作者,文章的共同第一作者是已毕业博士研究生邢荣荣和在读博士研究生郭展辰。
论文信息:
Molecular Imprinting and Cladding Produces Antibody Mimics with Significantly Improved Affinity and Specificity
Rongrong Xing#, Zhanchen Guo#, Haifeng Lu, Qi Zhang and Zhen Liu*
Sci. Bull. 2021, DOI: doi.org/10.1016/j.scib.2021.10.006