线粒体不仅是细胞进行有氧呼吸的主要场所,其在细胞凋亡中也发挥重要调节作用。线粒体功能障碍导致许多疾病的发生和发展,包括恶性肿瘤、心血管疾病、神经退行性疾病和代谢性疾病以及衰老等。因此,在疾病的治疗中通常将线粒体作为药物作用靶点。然而,由于存在各种生理和生物学屏障,将治疗药物特异性递送至细胞器较为困难。当前,亲脂性阳离子(例如三苯基TPP)通常用作线粒体靶向基团以将生物活性成分递送至线粒体,然而由于靶向效率低、肿瘤组织蓄积少和系统性毒性限制了其进一步的应用。值得注意的是,大多数线粒体蛋白是在细胞质核糖体上合成后重新定位到线粒体中以发挥后续功能。这种运输依赖于可产生线粒体靶向信号的线粒体前体蛋白(MPP),该蛋白在信号指引下转运到线粒体中。目前,可成功将蛋白质导入线粒体的已知MPP通常具有两个共同特征,即必需的同源氨基酸序列(包括精氨酸等)和两亲性N-末端区域。因此,设计具有特定氨基酸部分的分子以模拟MPP的关键序列是进行线粒体靶向递送的有效策略。
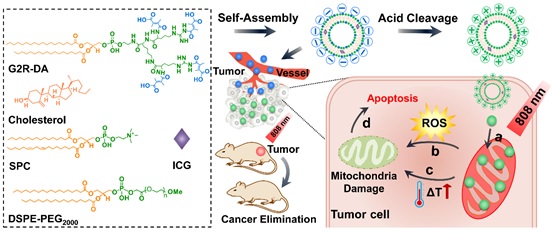
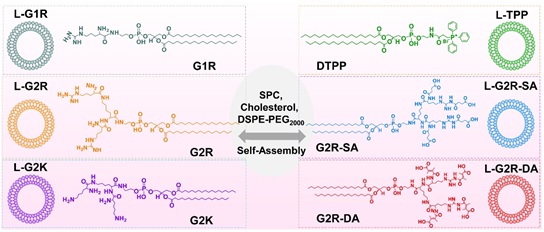
近年来,人们越来越多地致力于开发针对线粒体靶点的光热疗法(PTT)和光动力疗法(PDT)以治疗恶性肿瘤。由于线粒体对热休克很敏感,同时线粒体具有产生活性氧(ROS)的富氧细胞环境,是最适合PDT触发细胞凋亡的细胞器。本研究中,我们设计并构建了一系列基于精氨酸残基修饰的树突状脂肽分子(DLP)的线粒体靶向制剂,利用DLP作为信号传导和导向基团来实现药物的细胞器传递。为了模拟天然MPP中的基础氨基酸结构域,使用多精氨酸的树状大分子放大递送系统与线粒体的相互作用;另一方面,选择硬脂酰基作为疏水链段以增加亲脂性,强化两亲性载体与线粒体膜之间的亲和力。为了最大化药物在肿瘤组织的累积并最小化正常组织的摄取,具有肿瘤微环境响应性的2,3-二甲基马来酸(DA)修饰DLP,以阻断精氨酸的阳离子性质。最终,将DLP、大豆磷脂酰胆碱(SPC)、胆固醇、聚乙二醇-二硬脂酰磷脂酰乙醇胺(DSPE-PEG2000)和光敏剂吲哚菁绿(ICG)共组装制备线粒体靶向的脂质体(L-G2R-DA)。我们将TPP修饰的脂质体作为参比对照,在体外和体内系统地评估了PTT和PDT治疗恶性肿瘤的疗效。与TPP的线粒体靶向系统相比,基于树突状脂肽DLP的脂质体递送系统展现出高约3.7倍的线粒体靶向递送效率,在4T1乳腺癌小鼠模型中实现了肿瘤的根除治疗。
上述相关成果已以“Mitochondrion-specific dendritic lipopeptide liposomes for targeted sub-cellular delivery” 为题在Nature Communications(DOI: 10.1038/s41467-021-22594-2)在线发表。37000cm威尼斯16年入站博士后姜雷(现为中国药科大学副教授)为本文第一作者,蒋锡群教授为通讯作者。