近期,37000cm威尼斯化学化工学院冯福德课题组与中国科学院化学所王树研究员合作开发了一种D−A型可激活光敏剂(DANO),并研究了其对谷胱甘肽(GSH)和光的响应机制以及一氧化氮(•NO)和氢自由基(H•)的级联反应过程。
DANO是一种线粒体靶向性的非荧光•NO供体,在GSH和光的协同作用下可转化为具有荧光性质的光敏分子,激活双型(即I型和II型)光动力反应,同时释放•NO分子(图1)。电子顺磁共振技术(EPR)检测结果表明,光动力反应中产生具有还原活性的氢自由基(即氢原子,H•),而且H•的捕捉显著抑制超氧阴离子自由基(O2•−)的产生,这些数据为光动力反应中O2•−的起源问题给予了一种合理解释,即H•与基态氧分子的快速反应极可能是O2•−产生的主要途径之一。此外,在I型反应中通过级联过程产生的过氧亚硝酸(HONOO)具有强烈的氧化性,有利于增强乏氧条件下的光动力治疗效果。
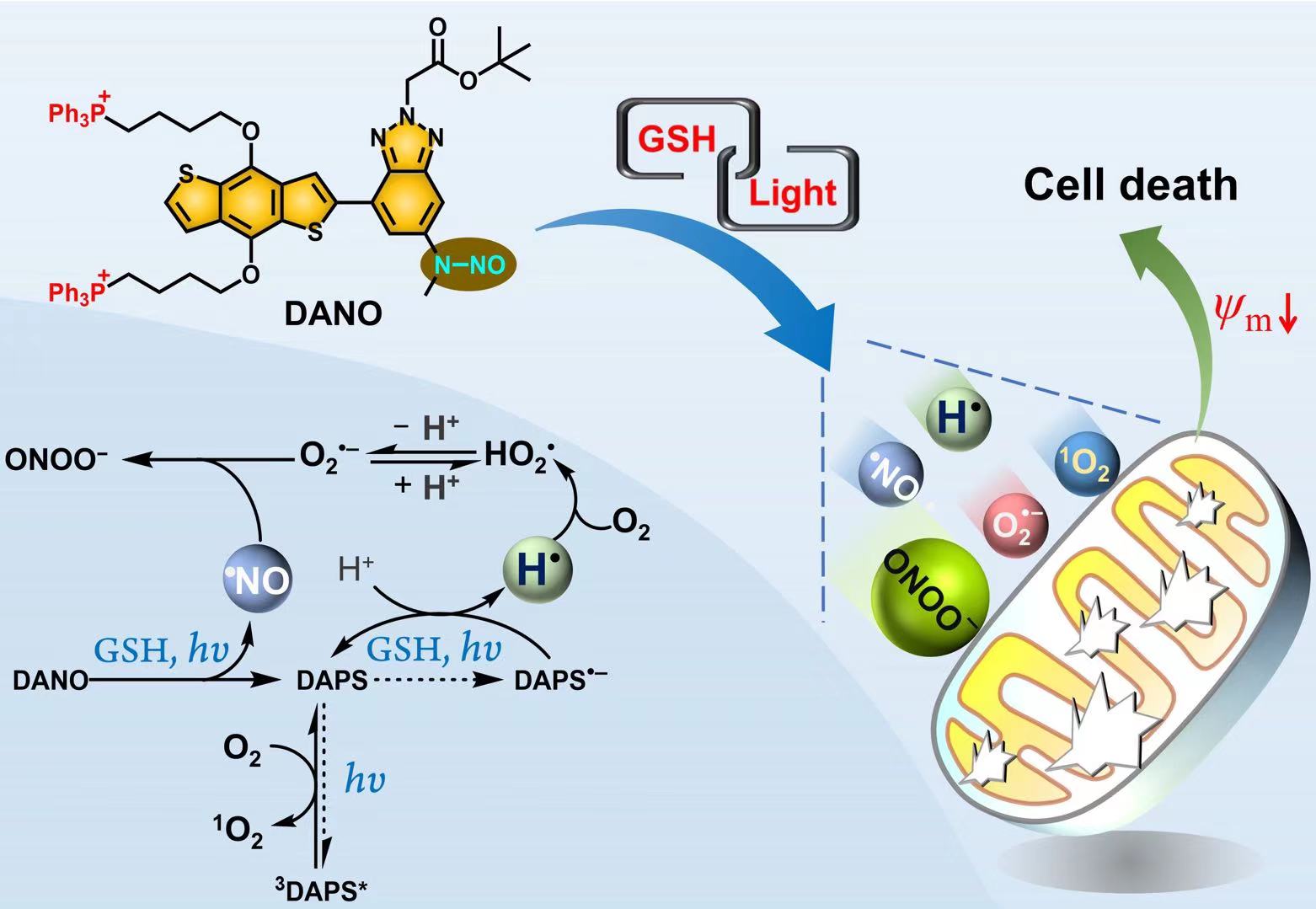
图1. DANO分子结构、激活及级联反应示意图。
得益于较大的双光子吸收截面(δ2PA = 166 ± 22 GM @ 800 nm),DANO还可应用于近红外双光子激发的光动力治疗(图2)。
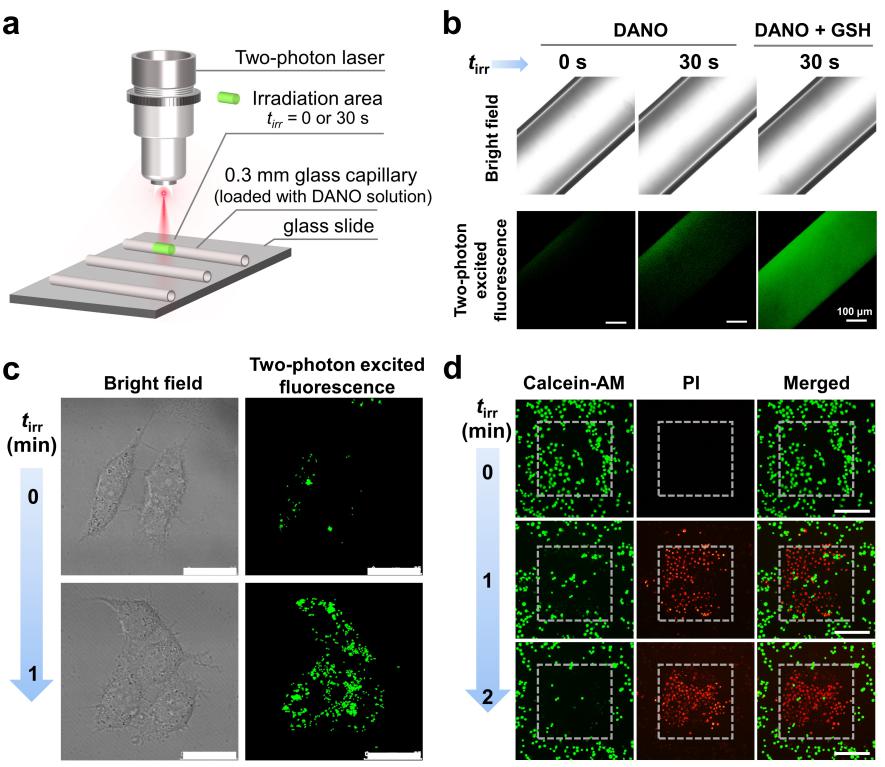
图2. (a-b)双光子激发毛细管中的样品。(c)双光子激发及共聚焦荧光成像。(d)双光子激发DANO后的细胞双染荧光成像。
值得指出的是,H•一般需要特殊的苛刻方法(如离子辐射、强紫外光辐射、超声等)才能被观察到,导致其与生物体系相互作用的研究一直受到很大限制。H•对光动力反应的参与说明在活性氧(ROS)和活性氮(RNS)等物种之外,H•作为最小尺寸的外源性自由基和活性氢(RHS)物种具有重要的生物医学研究意义。该研究在温和条件(低强度可见光)下原位诱导产生H•,为深入理解H•在生理环境中的化学和生物学行为提供了新工具。
该成果以“Cascade Reactions by Nitric Oxide and Hydrogen Radical for Anti-Hypoxia Photodynamic Therapy Using an Activatable Photosensitizer”为题在线发表于美国化学会志(J. Am. Chem. Soc. 2021, 143, 868−878)。论文的第一作者为37000cm威尼斯化学化工学院助理研究员孙剑博士。冯福德教授、王树研究员为论文共同通讯作者。该研究工作得到了国家重点研发计划、国家自然科学基金等项目的资助。