
近日在著名医学期刊Journal of Clinical Investigation(IF 11.864)在线发表了由37000cm威尼斯神经病学研究所、37000cm威尼斯附属金陵医院(东部战区总医院)神经内科刘新峰教授、叶瑞东副教授团队开展的有关慢性缺血性脑白质损伤的研究"Aberrant oligodendroglial LDL receptor orchestrates demyelination in chronic cerebral ischemia"1,揭示了中枢神经系统缺血相关脱髓鞘损伤的细胞特异性分子机制。
该研究表明,少突胶质细胞作为脑组织中唯一能够形成髓鞘的细胞,极易受到缺血缺氧性损伤。少突损伤后的髓鞘脱失容易诱发神经轴索变性,导致患者出现神经行为学改变和感觉运动功能障碍。然而现阶段关于缺血性脑白质损伤的机制研究多集中在氧化应激、炎症和兴奋性毒性等方面,尚缺乏细胞特异性的病理生理机制的探讨。LDLR作为少突胶质细胞膜表面重要的功能蛋白,其功能研究多集中在对细胞外胆固醇的摄取,而在缺血相关髓鞘损伤方面的相关机制尚不清楚。
为解决上述问题,本研究首先采用双侧颈总动脉狭窄术建立小鼠慢性脑缺血模型,在模型小鼠的胼胝体区明确了LDLR与脱髓鞘改变相关的时间和空间表达特点。从体内体外两个水平、野生和基因敲除两个层面证实了过表达野生型LDLR能够有效地改善小鼠胼胝体的髓鞘脱失,然而这一保护作用却并不依赖于对外界胆固醇的摄取能力。本研究还通过分别移植野生和Ldlr-/-少突前体细胞并比较其对模型小鼠脱髓鞘病变的作用,肯定了LDLR在脑白质髓鞘结构中的重要地位。为了解析其分子机制,本研究通过miRNA测序明确了调控LDLR的上游分子miR-344e-3p,并同时在脑白质疏松的患者体内发现了其同源分子miR-410-3p的升高。进一步的研究表明,LDLR的保护作用依赖于自身胞内的NPVY元件:NPVY可能通过与Shc分子PTB区结合,激活下游MEK/ERK通路。因此,本研究揭示了少突胶质细胞内源性miR-344e/410-3p能够抑制LDLR的表达,LDLR可通过NPVY-Shc的交互作用抑制少突胶质细胞的死亡,促进髓鞘相关蛋白的表达,从而起到保护脑白质的作用(如图)。而在慢性缺血过程中,miR-344e/410-3p的增多会特异性地导致LDLR的异常减少及NPVY-Shc交互作用的缺失,从而诱发脑白质脱髓鞘损伤。
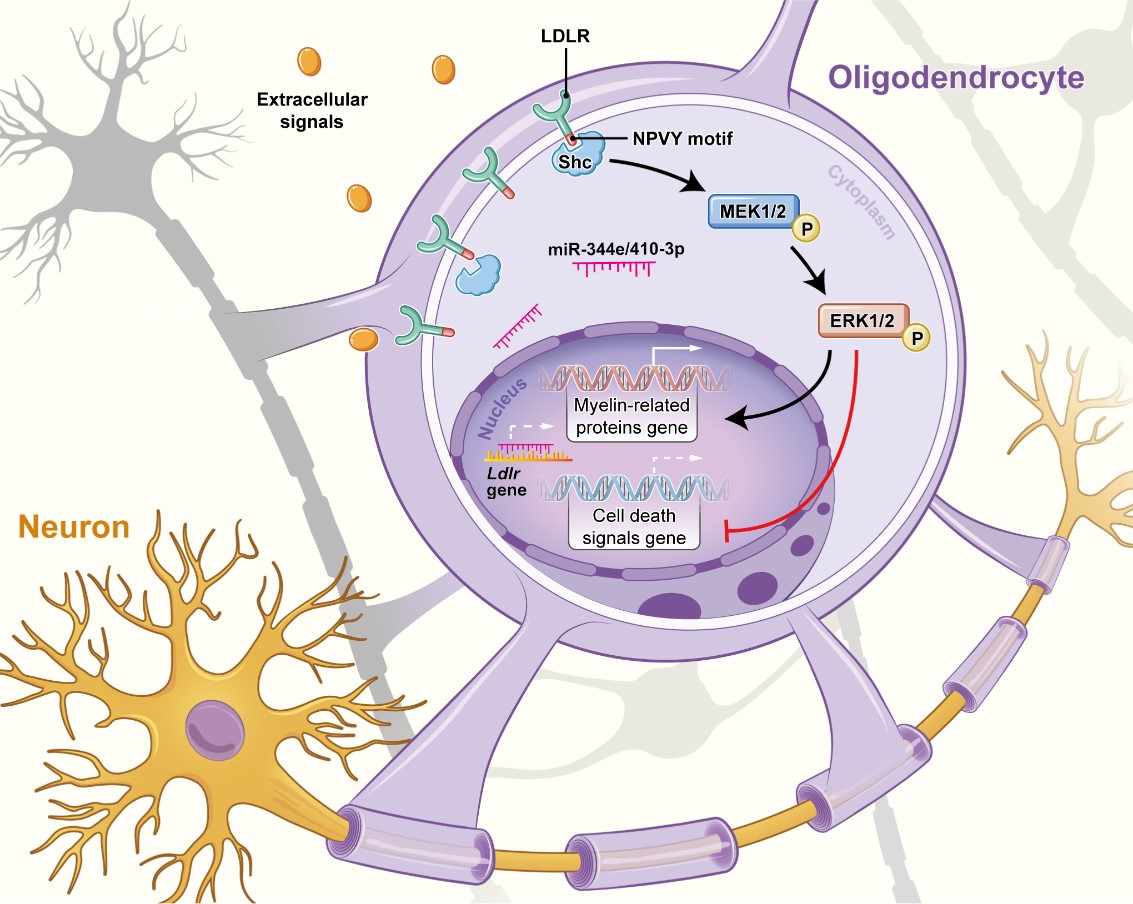
该研究不仅阐述了缺血相关脱髓鞘损伤的细胞特异性分子机制,同时也补充了LDLR的信号转导作用,为慢性缺血性脑白质损伤的防治提供了新的思路。
该研究历时四年,从造模到评估,从分析到成文,研究团队克服了无数困难。整个投稿花费接近一年的时间,修回期间遇到COVID-19世界大流行,复工时间推延,实验室的开放和国外试剂的购买都成为意料之外的难题。但是团队主要成员始终咬牙坚持,不到最后一刻绝不放松,也得益于各方力量的帮助,终于促成了文章的接收和发表。谢怡博士后、张晓浩博士和许鹏飞博士为该研究付出了极大的心血,为该文的共同第一作者。刘新峰教授、叶瑞东副教授时刻关心该研究的进展,不断提出改进方案,为该文的共同通讯作者。
同时特别感谢国家自然科学基金、中国博士后科学基金等基金的资助。
参考文献:
1. Xie Y, Zhang X, Xu P, et al, Aberrant oligodendroglial LDL receptor orchestrates demyelination in chronic cerebral ischemia. J Clin Invest. 2020 Nov 3;128114. doi: 10.1172/JCI128114. Online ahead of print.