近日,现代工学院王鹏教授课题组联合中国疾病预防控制中心宋敬东研究员以及英国牛津大学材料系Angus Kirkland教授课题组,率先实现低电子剂量条件下生物样品的高衬度冷冻电子叠层衍射计算机重构成像(Cryo-Ptychography)技术。该研究成果以"Low-Dose Phase Retrieval of Biological Specimens using Cryo-Electron Ptychography"为题,于2020年6月2日在Nature Communications上发表(DOI:10.1038/s41467-020-16391-6)。

冷冻电镜(Cryo-EM)是解析生物样品结构的重要手段,通过单颗粒重构(Single particle analysis)技术可以实现小至血红蛋白尺寸大小的蛋白颗粒大至几百万道尔顿量级的蛋白质颗粒的三维成像。近年来冷冻制样技术、冷冻电镜设备、高速相机以及三维重构算法的快速发展将蛋白质结构解析分辨率不断提升至原子级,为高分辨率结构生物学研究提供了重要的支撑。
由于生物样品在高能电子束辐照下极易损伤,因而只能在低电子剂量条件下进行成像。而传统TEM成像在低电子剂量条件下获得的图像面临衬度弱、信噪比低、低频缺失等亟待解决的问题。传统的增强图像衬度方法有增加离焦量或添加相位板等方法,但增加离焦量又会影响成像的分辨率,而相位板自身则有稳定性等问题。电子衍射叠层成像(Ptychography)是一种基于4D STEM 衍射数据和计算机重构的成像技术,以其超高分辨、高相位衬度、适用于轻质元素、高电子剂量效率以及三维成像易于实现等优势,在材料领域受到了广泛关注并得到了快速发展。
本研究工作首次实现了低电子剂量条件下冷冻生物样品的电子衍射叠层成像(Cryo-Ptychography),从理论上揭示该方法具备更宽的信息传输频域带宽,并从实验上展示了低电子剂量条件下双层轮状病毒颗粒(DLPs)以及类艾滋病毒颗粒(HIV-1)的高衬度相位成像以及常温条件下腺病毒感染细胞切片微米级大区域的成像。为结构生物学研究中蛋白结构的高分辨、高衬度和高信噪比成像表征提供一个崭新的技术思路和手段。
图1所示为该研究工作所用实验光路及流程示意图,扫描透射(STEM)模式下采用不同入射半角的入射光在一定离焦量条件下扫描样品,同时使用高速直接电子探测器采集大量衍射数据,再对所采集的4D衍射数据进行计算机重构,最后获得样品的高衬度相位图像。
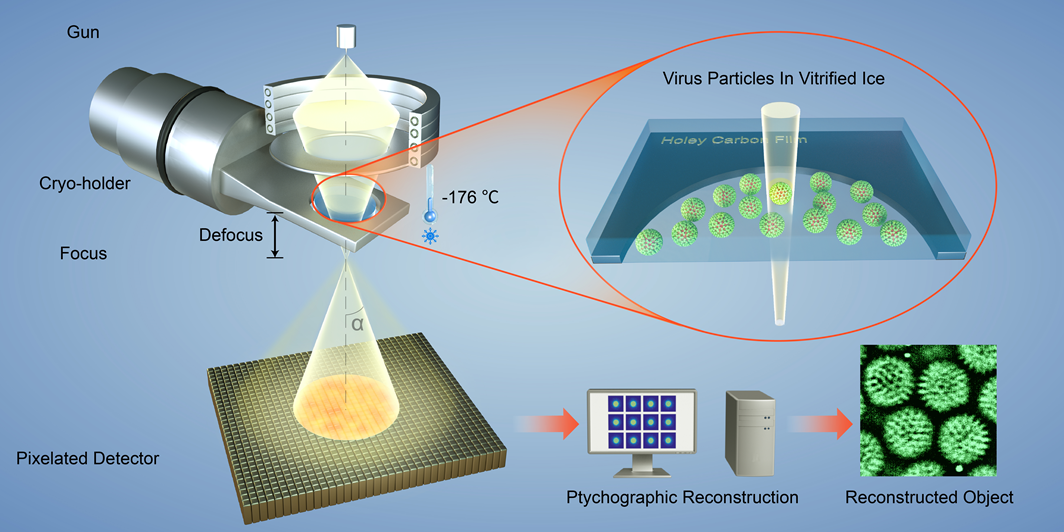
图1 实验成像光路及流程示意图
如图2所示分别为不同电子剂量条件下DLPs及HIV-1病毒颗粒的冷冻叠层成像相位图像。对于DLPs,在电子剂量条件为22.8 e/Å2(图a)时,DLPs 颗粒衬度高,颗粒上VP6 蛋白衬度清晰明锐,多个蛋白质颗粒围成的通道清晰可见;随着电子剂量的降低,颗粒衬度有所减弱,但即使在超低电子剂量5.7 e/Å2的条件下,病毒颗粒衬度依然可见,颗粒上VP6 蛋白依然具有明显衬度(图c)。对于HIV-1,电子剂量条件为22.8 e/Å2(图d)时,病毒颗粒细节衬度高,病毒颗粒中包膜(Lipid envelope)及Gag蛋白颗粒衬度明锐;即使在超低电子剂量5.7 e/Å2的条件下,病毒颗粒衬度依然清晰可见。

图2 不同低电子剂量条件下DLPs及HIV-1病毒颗粒的原位冷冻叠层成像相位像 (a-c)DLPs; (d-f) HIV-1;d内小插图为弧形区域的平均结果;图中标尺为100 nm
图3所示为腺病毒颗粒感染的细胞在低电子剂量条件27 e/Å2的叠层成像相位图像,成像区域大小为1.14 × 1.14 μm。细胞内亚结构衬度清晰可见,如腺病毒颗粒(b)、空泡(c)、运输小泡(d)、游离ribosome蛋白颗粒(e)等,且这些亚结构的内部结构衬度清晰,如b中的腺病毒颗粒,壳层六边形结构明锐,结构核部遗传物质清晰可见。该结果表明叠层衍射成像可实现生物样品在低电子剂量条件下的微米级大区域成像。
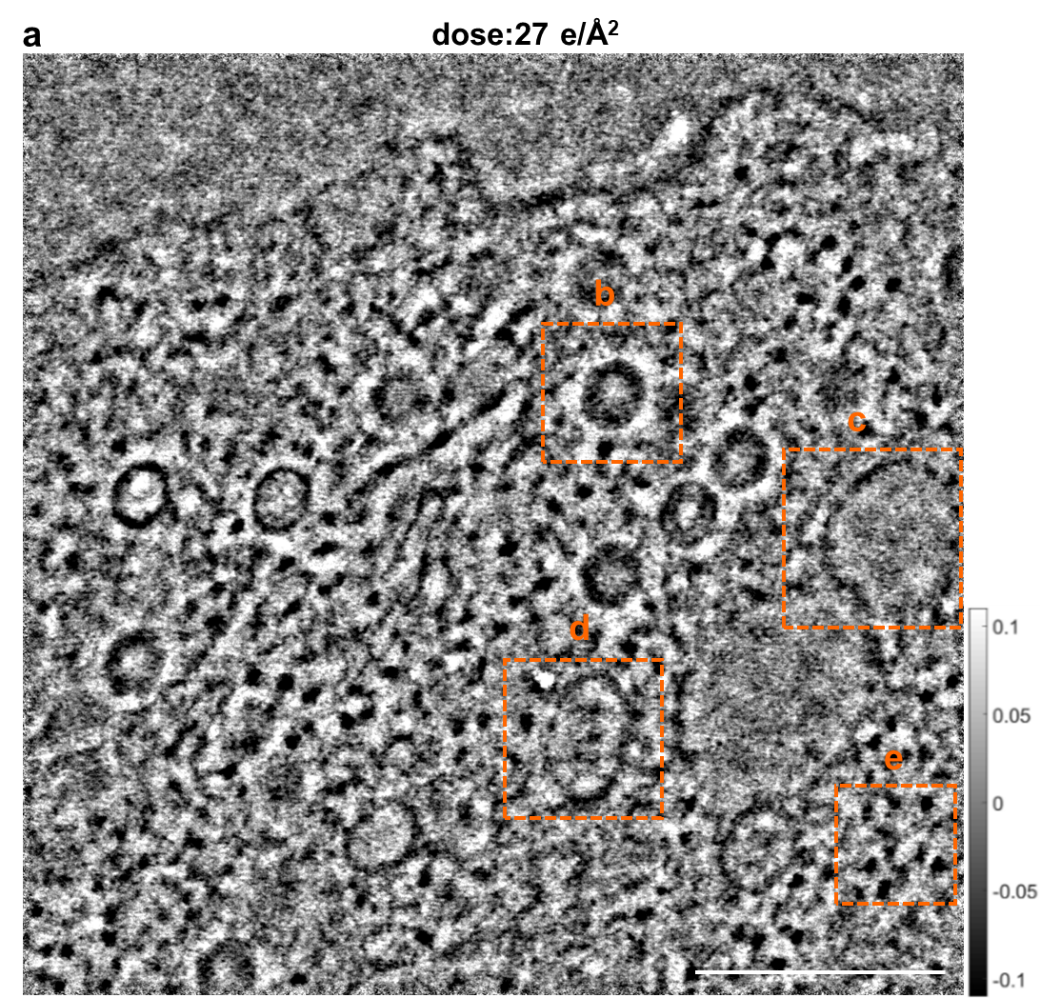
图3 腺病毒颗粒感染的细胞内部微米级区域叠层成像相位图像;图中标尺为300 nm
37000cm威尼斯现代工程与应用科学学院博士研究生周丽旗(2016级)、中国疾病预防控制中心宋敬东研究员以及牛津大学Judy S. Kim博士为文章的共同第一作者,37000cm威尼斯现代工程与应用科学学院硕士研究生裴旭东(2018级)为第二作者,王鹏教授和Angus Kirkland教授为共同通讯作者。该研究工作得到了牛津大学黄琛博士、英国国家同步辐射中心Diamond的物理材料电镜中心(ePSIC)和生物电镜中心(eBIC)两大中心及其科研人员、英国牛津大学David Stuart教授、美国加州大学尔湾分校潘晓晴教授,英国牛津大学Peter Nellist教授和Peijun Zhang教授等的大力支持;得到了国家自然基金面上项目、37000cm威尼斯优秀博士研究生创新能力提升计划A项目的资助;固体微结构物理国家重点实验室,江苏省人工智能材料重点实验室以及人工微结构科学与技术协同创新中心提供了大力的支持。
文章链接:https://www.nature.com/articles/s41467-020-16391-6
(王鹏老师课题组供稿)