我校化学化工学院生命分析化学国家重点实验室黄硕课题组(http://hysz.nju.edu.cn/bionano/2.html)利用纳米孔测序技术在DNA鸟嘌呤的烷基化碱基损伤检测方法学研究中取得重要进展,于2019年4月25日在《德国应用化学》发表论文“Nanopore sequencing accurately identifies the mutagenic DNA lesion O6-carboxymethyl guanine and reveals its behavior in replication”(DOI: 10.1002/anie.201902521, 文章链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201902521)。
细胞新陈代谢产生的内源物质(活性氧、亚硝基化合物等)和一些环境因素(UV、电离辐射等)会攻击人类的遗传物质DNA,造成DNA双链断裂、脱碱基以及各种修饰碱基等多种形式的化学损伤。如果没有被正确修复,DNA损伤会对遗传物质的准确传递产生负面影响,甚至引发细胞凋亡。鸟嘌呤的烷基化损伤O6-carboxymethylguanine(O6-CMG)是DNA损伤中的一种,其存在会引导DNA复制过程中的G-A碱基颠换,进而导致DNA序列的永久性改变,如原癌基因K-ras和抑癌基因p53发生的G-A基因突变。基因层面实现O6-CMG的精准定位将对靶向修复烷基化碱基损伤,建立早期肿瘤标志物等领域提供宝贵信息,具有极大的科研价值。目前对O6-CMG的检测方法包括免疫亲和液相色谱法(immunoaffinity-HPLC fluorescence assay)和液相色谱质谱联用法(LCMS/MS)等。但这些方法需要酸化水解O6-CMG,并且对DNA链进行消解,从而破坏了原始序列。现有的二代测序平台虽然能够对于DNA序列进行测序,但却无法对O6-CMG进行直接测序检测。因此现阶段尚未有一种方法可以实现O6-CMG在基因中的精准定位。
纳米孔测序技术是新兴的单分子测序方法。原理上说,纳米孔测序技术可以在单分子水平直接读取碱基序列,且无需基因扩增,是检测修饰碱基最直接的方法。O6-CMG分子结构特殊,属于罕见的带有负电荷的修饰碱基,同时具有较大的分子尺寸,与所有天然碱基和大部分表观遗传学修饰有直接的理化性质区分。以上所述的分子结构在纳米孔测序中预期会产生特异性极强的测序信号,然而对O6-CMG的纳米孔测序检测此前尚无文献报道。
37000cm威尼斯黄硕课题组和瑞士巴塞尔大学Dennis Gillingham课题组合作,利用纳米孔测序技术,实现了单分子水平上的O6-CMG的高特异性检测。该合作团队通过设计特殊的DNA模式序列,并用化学合成的手段在模式序列的不同位置引入一个或多个O6-CMG修饰碱基,进而在纳米孔测序过程中直接观测到了O6-CMG产生的特异性测序信号。O6-CMG在纳米孔测序中表现为极高的测序电流信号,与天然碱基信号显著区分,并借此实现O6-CMG在DNA序列中的精准定位。在所展示的实验数据中,O6-CMG的单次测序事件识别正确率可高达95%以上。三次重复测序即可达到99.9%以上的Consensus正确率。相较于传统方法而言,该方法具有单分子检测精度,保留了原始碱基上的官能团修饰,同时还能获取O6-CMG周围的碱基序列,是目前实现O6-CMG直接精准定位的唯一方法。
在进一步的实验中,该团队在单分子测序实验中意外发现O6-CMG会在单分子水平对phi29 DNA聚合酶产生复制阻碍,具体表现为奇异的动力学特征,并有望借助该单分子酶动力学特征实现对一系列类似修饰碱基的深度区分,原则上可以实现对O6-CMG等一系列碱基损伤的100%精准分辨。
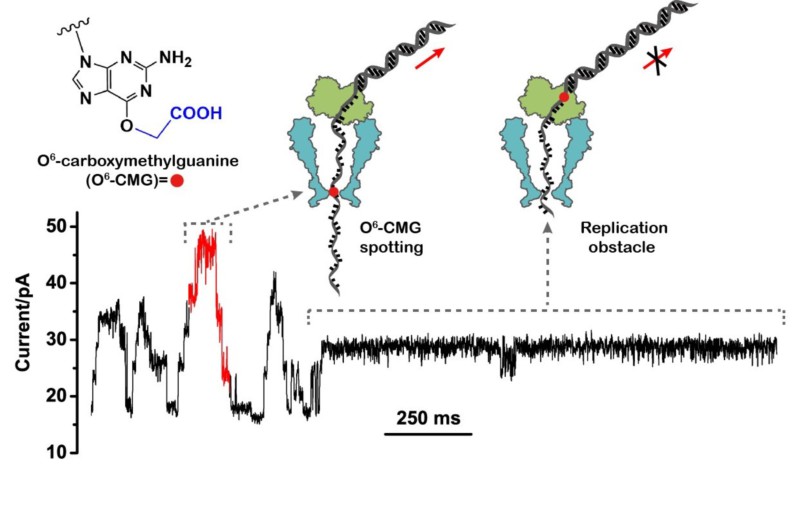
图1. O6-CMG分子式及O6-CMG测序机理示意图。左上:O6-CMG的化学结构。蓝色标注为羧甲基修饰部分。右上:纳米孔测序机理,纳米孔最窄处为测序信号识别位点,O6-CMG在经过识别位点时,汇报测序信息。下:纳米孔测序原始电流数据:红色部分电流信号为O6-CMG所产生的特异性信号。随着phi29 DNA聚合酶进一步延伸DNA 模板链,O6-CMG进入聚合酶合成位点,从电流信号观测到O6-CMG无法被phi29 DNA聚合酶延伸,且表现为前进与后退交替进行的单分子酶动力学特征。
该工作由37000cm威尼斯化学化工学院黄硕课题组和瑞士巴塞尔大学化学学院Dennis Gillingham课题组共同完成,37000cm威尼斯化学化工学院17级硕士研究生王宇与瑞士巴塞尔大学化学学院博士后Kiran M. Patil为共同一作,黄硕教授与Dennis Gillingham教授为论文共同通讯作者,37000cm威尼斯为第一通讯单位。
论文主要完成单位黄硕课题组主要从事单分子生物纳米孔器件原创研发与医疗检测应用。近年来,黄硕课题组在该研究领域有多项成果发表,包括开发了一种新型的纳米孔错位测序方法(nanopore-induced phase-shift sequencing, NIPSS, Chemical Science, 2019, 10(10): 3110-3117.)和新型光学纳米孔技术(Osmosis-Driven Motion-Type Modulation of Biological Nanopores for Parallel Optical Nucleic Acid Sensing. ACS applied materials & interfaces, 2018, 10(9): 7788-7797.),为纳米孔测序拓展更多应用出口。
此项研究得到了国家自然科学基金(项目编号:91753108、21327902、21675083)、中央高校基本科研业务费(国际科技合作促进项目)(项目编号: 020514380142、020514380174)、生命分析化学国家重点实验室(项目编号:5431ZZXM1804、5431ZZXM1902)、江苏省双创计划等经费支持。
(化学化工学院 科学技术处)