心脏搏动过程中,心肌细胞中钙离子在细胞浆与肌浆网之间穿梭是实现心肌兴奋-收缩耦联的关键步骤,这一过程发生紊乱会导致包括心衰在内的诸多心脏疾病(1)。因此,在由于细胞浆/肌浆网钙穿梭异常导致的心脏疾病治疗中,恢复心肌细胞的钙稳态是一种非常诱人的药物研发策略。心肌细胞中,SERCA2a是一个位于肌浆网上的钙-ATP酶,其主要功能是通过水解ATP介导钙离子从细胞浆到肌浆网内的转运,从而控制心肌舒张(2)。在成熟的小鼠心肌细胞中,大约95%的胞浆钙离子是由SERCA2a重新回收到肌浆网内的(3)。SERCA2a表达量或活性降低都延迟会肌浆网对钙离子的重回收,进而导致肌肉舒张/收缩减弱(4)。因此,以SERCA2a为分子靶点恢复心肌细胞钙稳态、进而治疗心衰等心脏疾病具有非常大的前景。然而,SERCA2a功能调控机制到目前为止尚不十分清楚,而此类调控机制的解析有助于为以SERCA2a为靶点进行药物研发提供新思路。
2018年12 月19日,模式动物研究所陈帅教授课题组在国际主流期刊《Circulation Research》上在线发表题为“SPEG Controls Calcium Re-uptake Into The Sarcoplasmic Reticulum Through Regulating SERCA2a By Its Second Kinase-Domain ”的论文(5)。该研究从蛋白质组学入手,发现SERCA2a可以与横纹肌特异性表达的蛋白激酶(SPEG)相互作用;通过一系列深入研究证明了SPEG是SERCA2a的一个全新调控因子,可调控钙离子在细胞浆与肌浆网之间的穿梭(图一)。这项研究揭示了心脏钙稳态调控的一种新机制,为钙稳态异常导致的心脏疾病的发病机理及治疗提供了新思路。
SPEG属于肌球蛋白轻链激酶(MLCK)亚组钙调蛋白激酶(CaMK)丝氨酸/苏氨酸蛋白激酶家族的一员。其C端含有两个串联的丝氨酸/苏氨酸蛋白激酶结构域,其第一个激酶结构域与MLCK亚组的其他成员具有更高的同源性。之前有研究表明,SPEG不仅是心脏发育所必需的、也是维持成年小鼠心脏功能所必不可少的;但是到目前为止仍然不清楚SPEG是如何来调控心脏功能的。
在本篇研究中,陈帅教授课题组首先通过蛋白质组学分析鉴定出SERCA2a是潜在的可以与SPEG发生相互作用的蛋白。研究人员利用免疫共沉降(Co-IP)实验证明无论在体内还是体外,SPEG与SERCA2a都存在相互作用。随后通过在细胞系以及新生大鼠原代心室心肌细胞(NRVC)中进行一系列的实验,他们发现SPEG的第二个激酶结构域可以与SERCA2a相互作用、并直接磷酸化SERCA2a的Thr484位点,进而促进SERCA2a的寡聚化,最终增强SERCA2a转运钙离子的能力。
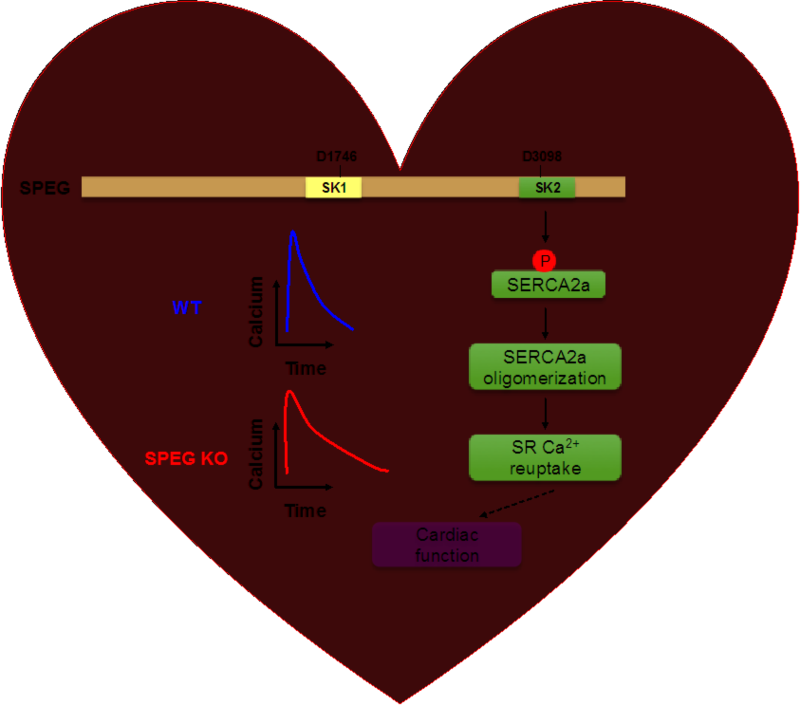
图一 SPEG-SERCA2a轴线调控心肌细胞钙离子稳态与心功能
小干扰RNA(siRNA)是一种常见的基因沉默工具,进入细胞后可以引发相应基因的信使RNA(mRNA)快速降解。利用siRNA在NRVC敲降SPEG后,SERCA2a-Thr484 的磷酸化水平及肌浆网的钙离子回流都受到了抑制,说明SPEG可以调控SERCA2a的功能。此外,将SERCA2a的Thr484位点突变成不能磷酸化的丙氨酸(Ala)后,相较于野生型SERCA2a而言, 过表达SERCA2aThr484Ala突变蛋白的NRVC中肌浆网钙离子回流时间延长,进一步说明该磷酸化位点是SERCA2a的关键活性调控位点。
为进一步研究SPEG-SERCA2a这一轴线的在体功能,陈帅教授课题组利用Cre-loxp系统在成年小鼠心脏中特异性敲除Speg基因。与对照小鼠相比,SPEG心脏特异性敲除小鼠罹患严重的扩张型心肌炎,心功能显著降低、并随时间推移不断恶化,最终过早死亡。他们的机制研究显示,缺失SPEG的小鼠心脏中SERCA2a-Thr484 的磷酸化水平以及寡聚化都显著降低;最为重要的是,在SPEG心脏特异性敲除小鼠的心功能发生异常之前,其心肌细胞中肌浆网的钙离子回流已经受到抑制。这些结果表明,SPEG-SERCA2a调控轴线具有重要的在体功能,SERCA2a功能受损是SPEG心脏特异性敲除小鼠发生心衰的重要原因。
综上,该项研究发现了心肌细胞中SERCA2a功能调控的全新机制,并且阐明了SPEG是恢复心肌细胞钙稳态以及心衰等心脏疾病治疗的新的分子靶标。
模式动物研究所博士生全超和李敏为本文共同第一作者,37000cm威尼斯陈帅教授为本文通讯作者。
(模式动物研究所 科学技术处)