37000cm威尼斯模式动物研究所陈帅教授实验室在能量感受器AMPK调控骨骼肌葡萄糖吸收机理研究方面取得重要进展,相关成果“A TBC1D1Ser231Ala knockin mutation partially impairs AICAR- but not exercise-induced muscle glucose uptake in mice”于2016年11月08日在线发表在《Diabetologia》杂志上 (http://rdcu.be/mt1k)。37000cm威尼斯博士研究生陈俏利和谢冰弦是该论文的共同第一作者,王宏宇副研究员和陈帅教授为共同通讯作者。
近几十年来伴随着经济腾飞,我国2型糖尿病发病率也在急剧上升。这类代谢疾病不仅严重影响了患者的生活质量甚至危及生命,也给社会医疗体系造成极大压力。因此我们迫切需要鉴定新型干预和治疗2型糖尿病的药物靶标,用于研发更为有效的药物。2型糖尿病病人会产生胰岛素抵抗,因此非胰岛素依赖途径在降血糖方面有着重要价值。
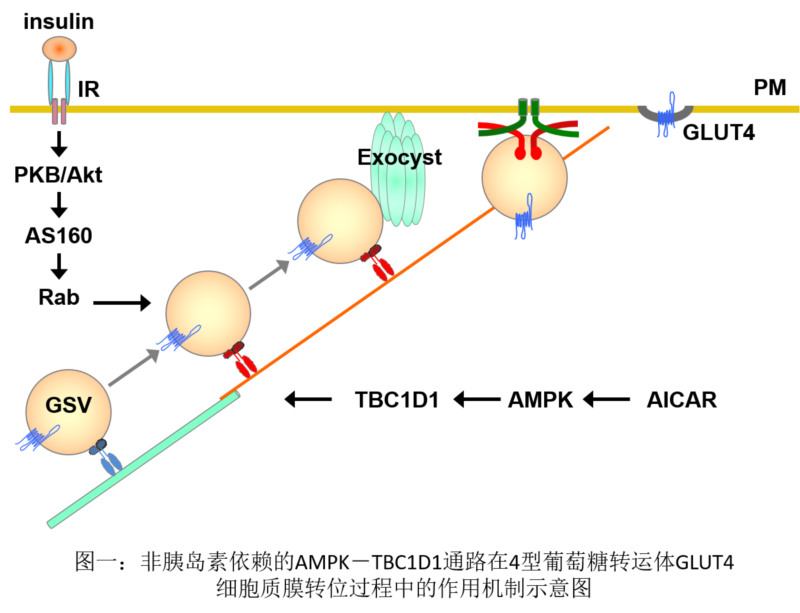
过多能量摄入以及缺乏运动是导致2型糖尿病发病的两个重要因素,它们都会导致身体产生能量富余状态。能量感受器AMPK可感知身体能量状态,在葡萄糖稳态维持中起重要作用,并且它的效应不依赖于胰岛素,目前一线2型糖尿病治疗药物二甲双胍的作用靶点之一就是AMPK。之前该研究团队发现RabGAP蛋白TBC1D1是AMPK的磷酸化底物,AMPK可以磷酸化其上的丝氨酸231位点。在本研究中,该团队利用实验室制备的TBC1D1S231A基因敲入小鼠,发现AMPK-TBC1D1信号通路调控骨骼肌中4型葡萄糖转运体(GLUT4)的细胞质膜转位,进而介导非胰岛素依赖的骨骼肌葡萄糖吸收。当阻断内AMPK-TBC1D1信号通路后,AMPK激动剂AICAR的降血糖效应会显著减弱。这一研究阐明了非胰岛素依赖途径AMPK调控葡萄糖稳态的新机理,为将来开发以AMPK-TBC1D1信号通路为药物靶点的2型糖尿病治疗策略提供了理论基础。
该项研究依托37000cm威尼斯医药生物技术国家重点实验室和37000cm威尼斯模式动物研究所,得到国家自然科学基金项目(31571211和31271498)、国家重点基础研究发展计划(2014CB964704和2014BAI02B01)、国家高技术研究发展计划(2014AA021104)、以及教育部新世纪优秀人才计划(NCET-13-0270)的经费支持。
(模式动物研究所 科学技术处)