骨科领域一直以来有两个很难解决的问题:1、难愈合骨折如老年性骨质疏松骨折的修复还没有很好的应对办法;2、骨折金属内固定物需要二次手术取出,这样会增加病人手术痛苦和经济负担。目前中国已经进入老龄化社会,老年性骨质疏松骨折发生率将大大增加,其社会和经济负担在医疗资源仍然短缺的中国会成为突出的问题。
自上世纪初金属镁进入工业量产时就被当时欧洲的骨科医生尝试用做骨折内固定材料。但当时生产的镁金属纯度不高,在体内会快速降解,造成较大的组织反应以及材料本身的破坏。2006年以来,国际镁金属研究的主要科学家如北京大学工学院的郑玉峰教授和德国柏林大学医学院的Frank Witte教授尝试用合金镁来延缓镁的快速降解。在观察动物体内镁合金材料降解速度的实验中,包括香港中文大学医学院秦岭教授在内的很多课题组都发现镁金属在动物体内有很强的成骨效应。镁为什么会有如此强烈的成骨效应——成为材料学界和骨科学界非常关注的问题。很好地解释这个问题无疑对可降解镁金属在骨科的临床应用奠定基础,并将激发更多针对骨科可降解材料的研究设计,会进一步发展出避免骨折二次手术的新的临床手术范式,从而催生出全新的医用材料产业。
张翼峰等人发现金属镁植入大鼠股骨骨髓腔后,在股骨外周形成大量的新生骨。由于新生骨组织位于骨膜下方,所以研究者推测骨膜组织主导了镁的成骨作用。骨膜组织分布有大量的感觉神经纤维和干细胞,骨膜神经纤维发端于脊髓背根神经节,能够感受温痛觉,释放具有标志性的神经递质降钙素基因相关肽(CGRP)。通过破坏大鼠股骨的感觉神经纤维,以及用基因和药物方式阻断外周神经递质CGRP在骨组织的受体,几种方式共同证明镁金属体内降解产生镁离子在骨膜部位刺激感觉神经末端释放更多的神经递质(主要为CGRP),骨膜内增多的CGRP进一步促进骨膜内干细胞的成骨分化,最后在骨膜部位形成大量的新骨。在体外实验中,研究者发现高于生理浓度的镁离子可以显著提高脊髓背根神经元的突触可塑性(使得神经囊泡大量聚集在突触末梢),该现象是体内镁金属影响感觉神经末端神经递质释放的细胞学基础。
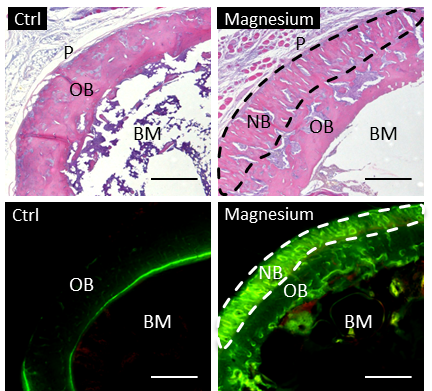
图一、镁金属在体内的成骨效应
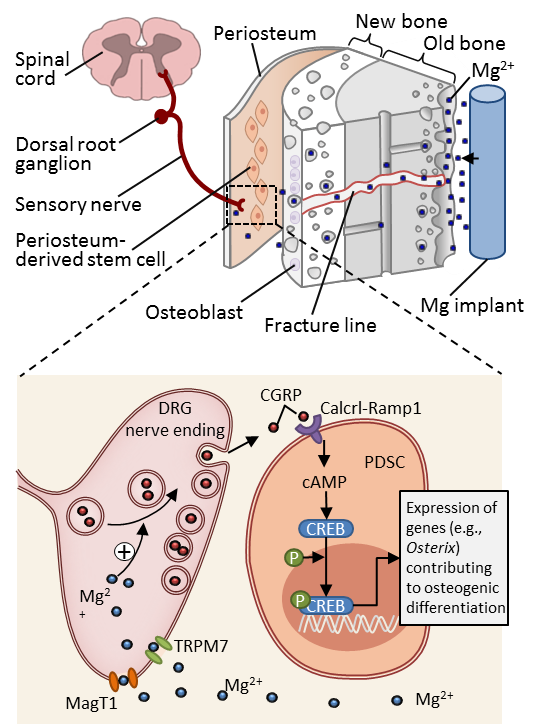
图二、镁金属成骨机制示意图
老龄动物体内感觉神经内的神经递质CGRP含量较年轻动物呈明显下降趋势,这也可能是老年性骨质疏松发生的原因之一。研究者在大鼠骨质疏松闭合性骨折模型中验证镁金属在骨折愈合中的促进作用。虽然纯镁或镁合金本身的强度可以支持动物骨折固定,但随着体内降解,其强度会在较短时间内下降,从而难以持续固定骨折断端。为此,研究人员设计了中空的不锈钢针管,将镁针置入管内,用该针管固定大鼠股骨骨折。在针管的骨折线部位开出孔洞,使得管内镁针降解后的镁离子释放到骨折断端部位。体内实验证实镁金属确实显著促进大鼠骨质疏松骨折的愈合。

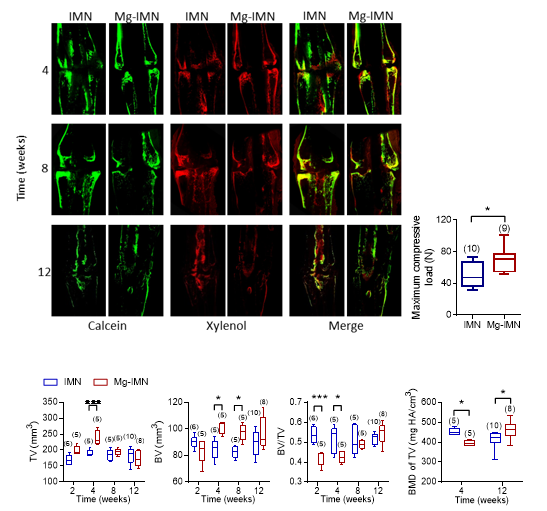
图三、含镁针不锈钢针管设计及骨折固定愈合效果
本研究很好地解释了镁金属体内成骨作用的机理,揭示了外周感觉神经在骨代谢中的关键作用,并首次在动物骨折模型中用镁金属促进了骨折的愈合。该项研究为可降解镁金属在骨科的临床应用奠定了理论基础。目前张翼峰博士所在的37000cm威尼斯医学院蒋青教授课题组已经与南京师范大学化学与材料学院朱丹教授课题组、北京大学工学院郑玉峰教授课题组展开合作,对镁金属降解行为进行可控设计。后续研究将克服纯镁及镁合金短期内快速降解的缺陷,保持镁金属材料在体内形态和力学性能的完整至骨折愈合完成。课题组有望尽快能够设计出直接用于人体骨折固定的可降解镁金属内固定材料,避免二次手术,减轻病人痛苦和经济负担。
文章合作者(共同第一作者)为香港中文大学医学院许建坤博士、阮晔纯助理教授,通讯作者为香港中文大学秦岭教授和北京大学郑玉峰教授。在此,张翼峰博士向本项工作的所有参与者致谢!
正文链接:http://www.nature.com/nm/journal/vaop/ncurrent/full/nm.4162.html
(医学院 科学技术处)