37000cm威尼斯医药生物技术国家重点实验室(生命科学学院)张辰宇教授课题组在皮下脂肪发挥功能分子机制的研究中取得重要进展,相关研究成果“Fasting induces a subcutaneous-to-visceral fat switch mediated by microRNA-149-3p and suppression of PRDM16 ”在线发表在自然子刊Nature communications (2016 May 31;7:11533)上。博士生丁寒莹是论文的第一作者,姜晓宏副教授为该论文的通讯作者,张辰宇教授及其课题组助理研究员李菁为该论文的共同通讯作者。
随着肥胖的全球化,很多人到了谈“脂”色变的地步,因而忽略了脂肪组织所提供的很多重要生理功能。目前较为公认的定义肥胖的指标是BMI指数,然而,研究发现肥胖导致的疾病与脂肪堆积的位置密切相关。内脏脂肪的过度累积易导致糖尿病、心血管疾病等一系列代谢性疾病的发生发展;而皮下脂肪的堆积除了影响美观,与以上疾病并未体现出直接相关性,因而被称为“健康的脂肪”。因此,研究脂肪组织在不同生理情况下的调控机制,可以帮助我们进一步了解不同位置脂肪的生物学功能,并帮助我们寻找正确的治疗肥胖引起代谢性疾病的方法和靶点。
寒冷和饥饿是在人类在数百万年的进化过程中一直面临的挑战。脂肪最被熟知的功能就是存贮功能,在食物短缺时可以通过分解脂肪为机体提供能量;而近期研究指出,人体的皮下脂肪中有相当一部分“米黄色”脂肪细胞可以通过在冷环境中产生热量来维持体温,而这部分细胞在内脏脂肪中则很少有分布。以上研究已经从分子层面证明了皮下脂肪与内脏脂肪的功能有显著差异,但是在饥饿情况下,这两部分脂肪的功能又有怎样的不同尚无报道。
在本研究中,张辰宇课题组发现,皮下脂肪除了具有“褐色化”以抵御寒冷的能力,还能够在饥饿的时候向“白色化”方向转变以保存能量,并明确了其分子调控机制;揭示出皮下脂肪在不同生理状态下通过其强大的可塑性,维持机体能量平衡的生物学功能 (Fig. 1.)。另外,他们发现“间歇性禁食”能够显著降低有害的内脏脂肪而非皮下脂肪,进一步显示了皮下脂肪“白色化”是对禁食引起的生理应激的一种适应性反应, 并证明了这种减肥方法的科学性。此外,他们发现可以通过在皮下脂肪中抑制miR-149-3p的表达激活其中的“米黄色”细胞,从而提高全身的能量消耗;较之全身服药可能引起的副作用,本研究提供了更为安全的治疗肥胖的潜在策略。
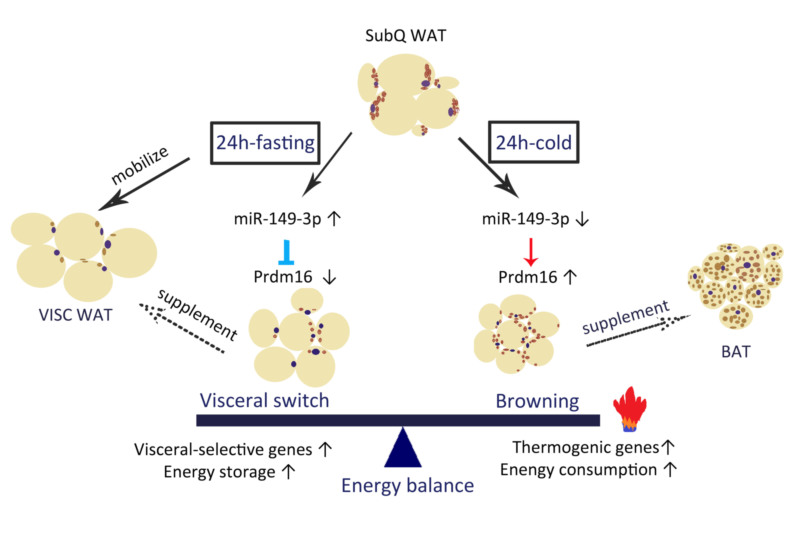
Fig.1. 不同生理条件下miRNA-149-3p调控皮下脂肪褐色化/内脏化
该项研究依托37000cm威尼斯医药生物技术国家重点实验室,37000cm威尼斯生命科学高等研究院,37000cm威尼斯生命科学学院,得到国家自然科学基金项目(No.81200201,81550001,81250044和31301060)、以及国家重点基础研究发展计划(2014CB542300号)的经费支持。
(生命科学学院 科学技术处)