骨骼肌约占人体重的40%,是人体最大的能量代谢和分泌器官,并对其他组织的生理稳态和疾病进展起到关键的影响。肌肉与骨骼从发育到整个生命周期中都保持着紧密的联系。在小鼠和人类上的大量研究表明,肌肉功能障碍和骨骼疾病的发展有着非常强的相关性。相反,运动在改善肌肉功能的同时也可以增强骨骼健康。虽然沃尔夫定律描述了肌肉和骨骼之间的机械相互依赖,但机械负荷的减少,如肌肉萎缩的情况,并不能完全解释骨丢失的现象。实际上,骨量可能受到来自肌肉的因子调节。有充分证据表明,从肌肉中释放的多种肌细胞因子和代谢产物可以以自分泌、旁分泌和内分泌的方式发挥作用。尽管临床数据已表明肌肉功能障碍和骨质丢失之间存在紧密的联系,然而,这两者间的因果关系及其潜在的生物学机制仍然扑朔迷离。
甘振继教授课题组从临床罕见疾病出发,应用基因组学、蛋白质组和生物信息学探究。意外发现仅局部骨骼肌功能障碍的肢带型肌营养不良(LGMD)病人存在全身系统性的骨量丢失,并发现这与肌肉线粒体质量控制蛋白FNIP1的病理性下调密切相关。借助功能获得与功能缺失的遗传小鼠模型,作者进一步证实了肌纤维中FNIP1的减少对骨代谢具有显著的不利影响。具体来说,肌纤维内FNIP1的特异性缺失会导致骨量减少及机械性损伤,而恢复肌纤维FNIP1的表达则能有效逆转这一趋势,凸显了FNIP1在维持骨量中的关键作用。紧接着,研究者通过多组学分析、小鼠模型和细胞模型的综合应用,进一步证实了IGF2是肌纤维FNIP1下游调控的促破骨分泌因子。体内外实验均证实,IGF2能够促进破骨细胞的分化,而体内过多的IGF2则会破坏骨代谢平衡,导致骨量减少及机械性损伤。最后,研究者发现在男性和女性患者中,血清IGF2水平与各种骨相关参数均呈现出显著的负相关性,揭示了IGF2在人类骨骼健康中可能发挥的关键作用。该研究发现了一种全新的肌肉-骨骼相互作用机制,即线粒体质控蛋白FNIP1的缺失会诱导转录因子TFEB的核转位,进而激活Igf2基因的转录及其后续分泌过程。随后,这种由肌肉分泌的IGF2通过IGF2受体(IGF2R)信号通路在破骨细胞中发挥作用,刺激破骨细胞分化并导致骨质疏松的发生。值得一提的是,新发现的促破骨分泌因子IGF2不仅与LGMD罕见病人相关,还与常见的老年性骨质疏松症的发生密切相关。
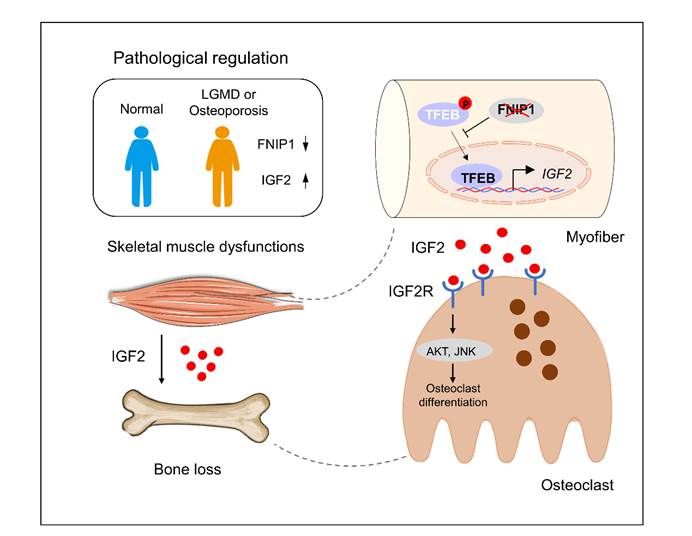
肌-骨对话轴调节肌源性骨病发病新机制 头图
该研究发现了一个全新的肌-骨对话轴介导肌源性骨质丢失发生;揭示了IGF2作为促破骨肌肉分泌因子新的重要功能;提出了FNIP1-TFEB-IGF2信号轴是肌肉疾病和骨质疏松症的潜在干预靶标。
2024年6月5日,37000cm威尼斯医学院甘振继教授课题组联合医学院附属鼓楼医院朱泽章教授课题组和复旦大学附属儿科医院李西华教授课题组在Science Translational Medicine长文发表了题为“ Muscle-bone cross-talk through the FNIP1-TFEB-IGF2 axis is associated with bone metabolism in human and mouse”的研究成果。此项工作发现了肌-骨对话轴调节肌源性骨病发病新机制,这一肌-骨信号轴可能成为治疗肌肉疾病和骨质疏松症的潜在靶点。37000cm威尼斯医学院博士研究生毛岩,南京医科大学博士研究生靳祯为本文的共同第一作者。37000cm威尼斯医学院甘振继教授,37000cm威尼斯医学院附属鼓楼医院朱泽章教授和复旦大学附属儿科医院李西华教授为本文的共同通讯作者。该项研究得到了国家自然科学基金委、科技部、教育部、江苏省科技厅以及中央高校等基金的支持,并在相关研究方面得到合作实验室的大力协助与支持。
原文链接:https://www.science.org/doi/10.1126/scitranslmed.adk9811