“饿不死”的肿瘤能被“撑死”吗?肿瘤对营养的争夺是其不变的特征,而且是其转移和恶化的关键。因此,几十年来,无数研究者试图通过限制营养来饿死肿瘤。例如,控制患者糖脂摄入,抑制肿瘤的新生血管、手术进行肿瘤血管栓塞,以阻断肿瘤细胞营养供应,但是都收效甚微。因为,肿瘤细胞自身可以通过不断突变、侵袭或转移来重塑其对营养的争夺能力,变得更加恶性。而且80%的肿瘤患者会出现营养不良,半数患者会发展为恶液质,表现为骨瘦如柴、极度无力,其中20%死于恶液质。这使得我们不得不重新对“饿死肿瘤”的策略进行思考。
37000cm威尼斯医学院胡一桥团队发现,与肿瘤细胞完全不同的是戈谢病(GD)细胞,在GD患者中,营养的摄入会加速GD细胞的死亡。GD是一种严重的遗传疾病,患者会出现发育迟缓、脑、肝及骨骼损伤,甚至死亡。GD是由于GBA基因突变,导致患者体内相关代谢酶功能障碍,造成摄入的糖和脂等营养在溶酶体聚集,使细胞代谢严重受阻而死亡。GD患者摄入的糖脂越多,代谢障碍越严重,细胞死亡越快。那么,能不能让肿瘤细胞也产生GD样的障碍呢,让营养掠夺性强的肿瘤细胞更容易死亡?
胆固醇是一种肿瘤细胞最喜欢的脂类营养物质,研究团队将一种含硼的胆固醇(CholB),与白蛋白非共价结合后,形成LDL样纳米粒(AbCholB)。利用肿瘤细胞对脂类营养的强争夺性,该纳米粒经表面LDL受体被主动摄入到肿瘤细胞内。进入细胞后,释放出的CholB可以通过硼酸基团与葡萄糖结合,产生类似GD细胞的糖苷化产物。这些糖苷化产物不断聚集,在溶酶体内形成微米级的结晶,导致溶酶体溶胀,产生类似GD的代谢障碍。而且,肿瘤恶性程度越高,对糖脂的需求越高,摄入的CholB和葡萄糖就越多,糖苷化产物聚集情况就越严重,造成的损伤也就越大。相反,正常细胞对糖脂的争夺能力较弱,受损很小。
团队的研究结果进一步阐明:在AbCholB诱导的GD样代谢障碍下,肿瘤细胞mTOR通路对营养感知钝化,处于长期稳定的抑制状态,肿瘤细胞无法感知营养饱和状态,最终被“撑死”。
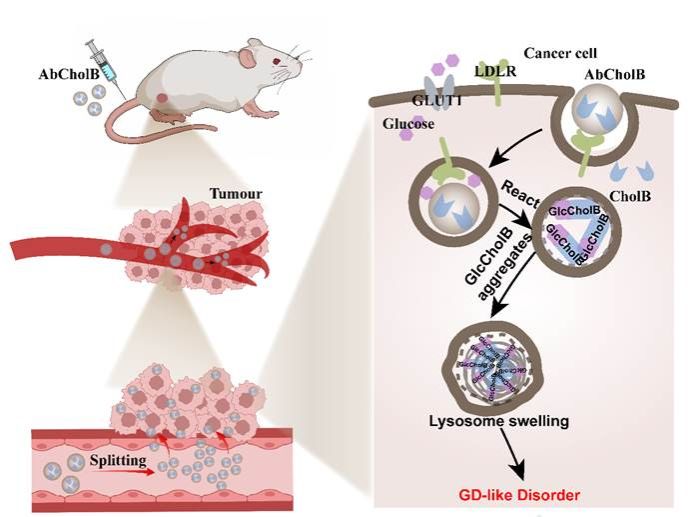
通过这种策略,团队排除了肿瘤突变所带来的异质性,充分利用了肿瘤细胞的共性‑营养争夺,避免了对正常细胞的严重损伤,提出了一种全新的肿瘤治疗方法。
2024年5月13日,医学院胡一桥团队在Nature Nanotechnology在线发表题为“Nanoparticles for Inducing Gaucher Disease-like damage in cancer cells”的研究成果。胡一桥教授为本文通讯作者;团队助理研究员岳春燕为论文第一作者,硕士研究生陆雯静和范书新为论文的共同第一作者;团队成员吴锦慧教授、袁阿虎副教授和董虹高级工程师均参与了该项工作。该研究获得国家自然科学青年基金等项目支持。

原文链接:https://www.nature.com/articles/s41565-024-01668-4