硼簇化合物,如闭式碳硼烷和巢式碳硼烷,是由硼、碳和氢元素构成的笼状化合物。碳硼烷具有许多独特的性质,如三维芳香性、高稳定性、高硼含量、低毒性和多中心多电子特性,因此在化学、药学、生物学、医学和材料学等领域得到了广泛应用。然而,由于硼簇中硼原子处于相似的化学环境,B−H键的选择性活化一直是合成挑战,这极大限制了其应用。
燕红课题组根据前期的研究基础即cage···π相互作用(Angew. Chem. Int. Ed. 2020, 59, 9018–9025),开发了一种新颖的碳硼烷官能团化模式,即通过设计一类非经典的cage···π类型的电子-给体/受体(EDA)复合物,其中三维的巢式碳硼烷为电子给体,二维的吖啶阳离子作为电子受体,在绿光照射下,这类EDA复合物可发生分子间的单电子转移(SET),生成巢式碳硼烷自由基,随后经过氢原子转移和亲核取代过程,选择性合成了一系列含有B–X(X = N,S,Se)键的碳硼烷衍生物(图1)。该反应由可见光驱动,具有反应条件温和、无需金属催化剂、空气中的氧气作为氧化剂、底物范围广、位点选择性好且反应产率高等优点,为选择性活化碳硼烷B–H键提供了新思路,有望推动碳硼烷药物分子和硼中子俘获疗法(BNCT)候选药物的合成和性质研究。
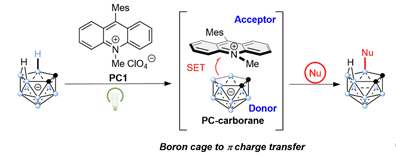
图1. 巢式碳硼烷B–H键官能团化新方法
作者首先尝试合成了cage···π类型的EDA复合物,并通过单晶衍射技术确定了其晶体结构(图2a)。同时利用稳态顺磁共振(EPR)技术捕获到了晶态下EDA复合物单电子转移的EPR信号(图2b)。 此外,作者还使用紫外可见吸收光谱和荧光发射光谱验证了EDA复合物内部的相互作用,如在晶体中EDA复合物与光催化剂相比,紫外可见吸收光谱发生红移 ~110 nm(图2c),荧光发射光谱有淬灭现象(图2d),进一步证实了晶态中的电子转移。在溶液中,通过滴定实验证明了巢式碳硼烷对光催化剂具有淬灭效应(图2e)。与光催化剂相比,复合物的紫外可见吸收光谱也发生了明显红移(图2f),表明溶液中也存在电子转移过程。这些实验结果为基于巢式碳硼烷与吖啶催化剂(PC1)形成的EDA复合物(PC-carborane)的电子转移提供了充分证据,为光催化反应设计提供了思路。基于对EDA复合物的理解,作者对催化反应进行了条件筛选,通过对不同光催化剂、波长、溶剂和添加剂的筛选,获得了最佳反应条件如下:在3 W绿光照射下,以巢式碳硼烷(0.1 mmol)、吡啶(0.2 mmol)、吖啶(5 mol%)、六氟磷酸铵(0.1 mmol)和二氯甲烷(2 mL)为反应体系,在室温空气中反应3小时,以90%的产率得到目标产物。
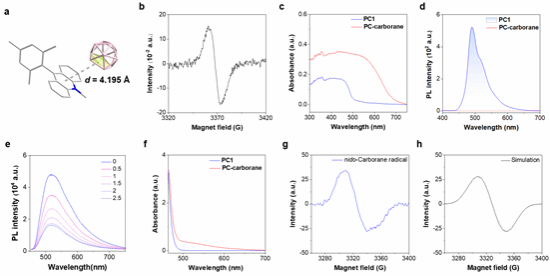
图2 各类谱学测定用于反应设计及机理验证
为了获得合理的机理理解,我们还需要证明自由基的产生,首先加入了TEMPO,的确能抑制反应发生,但无法分离加合物。此外,加入自由基捕获剂1,1-二苯乙烯,也未观察到自由基加成产物,表明是离域的硼笼自由基,而不是硼中心自由基。 通过稳态顺磁共振(EPR)技术很容易捕获到吖啶自由基,但仍然观测不到巢式碳硼烷自由基,表明该自由基反应活性高,在体系内浓度低,或者为短寿命瞬态自由基。清华大学郭兴伟教授用其最新开发的先进时间分辨EPR技术(U-PSD TREPR)成功捕获到巢式碳硼烷自由基(寿命~2.5 μs,g = 2.0047, 图2g)。这是首次通过EPR技术鉴定瞬态巢式碳硼烷自由基,理论计算模拟EPR也与实验结果吻合(图2h)。
另外,通过B–D–B氘代标记实验证明了氢原子转移过程。最终发现桥氘标记的原料生成的目标产物不含氘原子,表明桥氘在氧气或过氧化氢自由基作用下氧化离去,最后生成新的桥氢。由于同位素效应的影响,所得产物产率明显降低。
基于以上实验结果,作者提出了如下反应机理:即在绿光诱导下,巢式碳硼烷底物与吖啶催化剂经过非共价cage···π相互作用发生单电子转移,生成巢式碳硼烷自由基。随后,经过B–H–B氢原子转移(HAT)过程,生成高反应活性的中性硼笼中间体,其与亲核试剂反应生成B(9)位点取代产物(图3)。
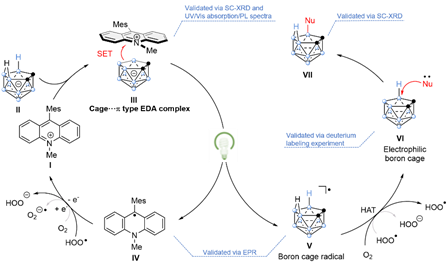
图3. 可行性反应机理
基于以上机理的理解,作者对不同巢式碳硼烷和吡啶衍生物(吡啶,嘧啶,吡嗪,喹啉等)进行了底物拓展,以中等至优秀的产率得到了一系列B–N偶联的碳硼烷基产物,反应位点单一选择B(9)位点(图4)。
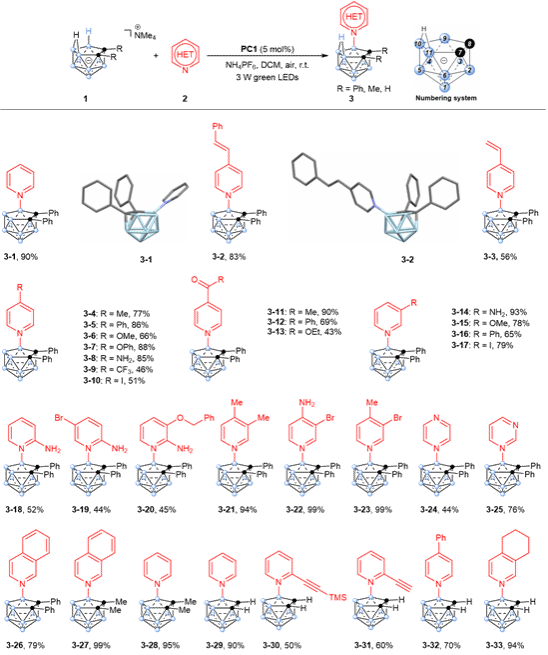
图4. B–N偶联碳硼烷基产物
另外,作者也对不同的咪唑衍生物(噻唑,噁唑,三氮唑,苯并咪唑等)以及亚胺进行了底物拓展,以中等至优秀的产率得到了一系列B–N偶联的碳硼烷衍生物(图5)。然后,作者又对不同的底物进行拓展如硫醚衍生物,硒醚衍生物和硫代酰胺衍生物等,以中等至优秀的产率得到了一系列B–S/Se偶联的碳硼烷衍生物(图5)。
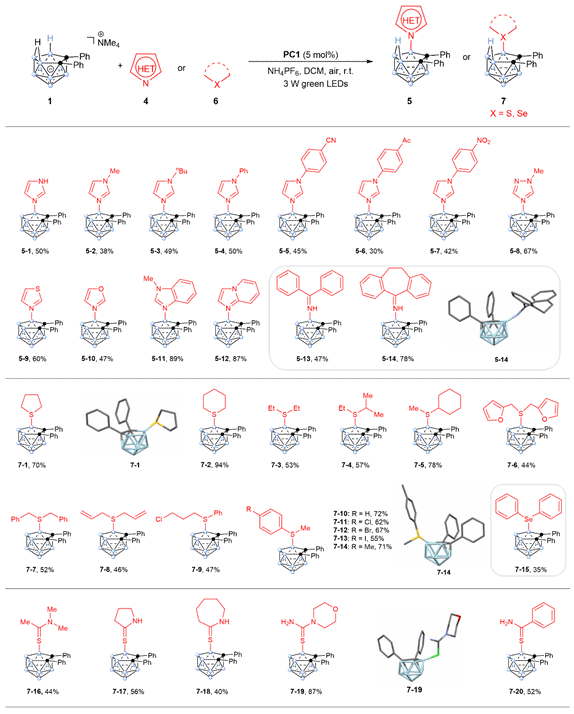
图5. B–N/S/Se偶联的碳硼烷基产物
最后作者应用该策略,以高产率获得了巢式碳硼烷和不同药物分子之间的直接偶联,包括与吡啶-氨基酸模块化分子的偶联(图6)。通过这种方法,也可合成一系列BNCT候选药物分子。此外,作者还筛选了其中一些产物分子,并进行了抗肿瘤活性实验,结果显示出良好的生物活性。这些合成的碳硼烷基分子或许具有更好的药物活性和选择性,以及更低的毒副作用,有望筛选成为新型抗肿瘤药物,因此该研究为碳硼烷相关化合物的合成和药物研究提供了新的思路和方法。
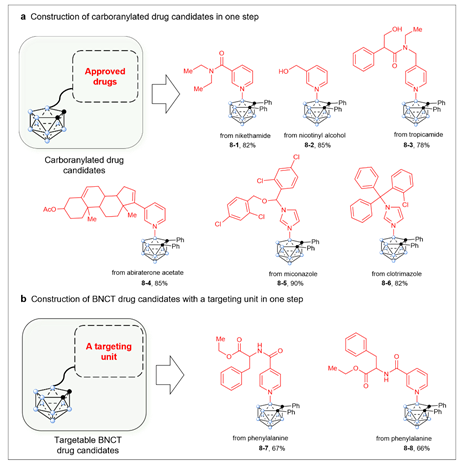
图6. 合成应用
作者首次报道了一种新颖的反应策略,通过简单的光诱导巢式碳硼烷的笼活化,实现了位点选择性的B–H官能团化。该反应具有许多优点,包括温和的反应条件(使用廉价的吖啶盐作为光催化剂,绿光激发,空气作为氧化剂,室温反应,反应时间短等),具有广泛的底物适应性(尝试了75个底物),产率高(可达99%),且具有单一的位点选择性(B9)位点)。因此,本研究不仅拓展了巢式碳硼烷的功能化方法,而且为碳硼烷基功能分子的合成提供了新路径。该研究的相关结果发表在J. Am. Chem. Soc. 2024, DOI: 10.1021/jacs.4c00550。
文章的第一作者是博士生徐圣文,通讯作者是燕红教授。巢式碳硼烷自由基捕获与清华大学郭兴伟教授课题组合作完成,理论计算与西班牙Prof. Jordi Poater (Universitat de Barcelona) 和 Prof. Miquel Solà (Universitat de Girona) 教授合作完成。该项研究得到了科技部国家重点研发计划和国家自然科学基金委重点项目资助。