衰老增加了阿尔兹海默病(Alzheimer’s disease, AD)等神经退行性疾病的风险,表现为神经再生能力、突出强度和功能降低等,但是衰老如何导致认知功能障碍的机制仍不清楚。有研究表明AD进展过程中的认知功能损伤和骨代谢异常具有显著相关性。近年来的研究发现,骨骼具有一定的内分泌功能,能够分泌多种骨源性因子调节骨外器官的稳态。但是,骨源性性因子是否参与衰老和AD过程中认知功能障碍仍未被揭示。
37000cm威尼斯医学院研究人员发现,与12月龄小鼠相比,22月龄小鼠认知能力下降并伴随大脑中Wnt/β-catenin信号传导失调,并且皮质和海马中Sclerostin水平显著升高。临床研究研究表明,男性和女性脑脊液中Sclerostin水平均随年龄增长而显著增加。同时,研究者证实Sclerostin能够穿过血脑屏障,并且衰老过程中增多的Sclerostin水平主要来源于骨组织。这一结果表明,骨源性Sclerostin水平的增加可能与衰老过程中大脑Wnt/β-catenin信号的失调有关。
研究者在Sost敲除小鼠的皮质和海马中检测到了较高的β-catenin水平和较低的BACE1水平,而SOST过表达小鼠中结果相反。同时,研究者发现,Sclerostin能通过Wnt/β-catenin信号促进神经元细胞BACE1表达和Aβ蛋白分泌。更重要的是,老年Sost敲除小鼠皮质和海马中的Aβ蛋白显著减少。这些结果表明,骨细胞分泌的Sclerostin可以抑制神经元中的Wnt/β-catenin通路,通过上调BACE1的表达来加速Aβ的产生。
研究者构建了AD小鼠模型(APP/PS1小鼠),通过慢病毒在骨细胞中上调Sost表达,发现慢病毒注射2月后血清和脑组织中的Sclerostin水平均升高,皮质和海马中β-catenin水平降低、BACE1水平升高,并且脑组织中淀粉样蛋白沉积增多。同时,慢病毒过表达Sost后,APP/PS1小鼠认知功能显著降低。上述结果表明,骨细胞来源的Sclerostin可以通过促进AD小鼠模型中的Aβ产生加快AD疾病进展。
研究者在老年人中发现,血清Sclerostin水平与认知功能呈负相关。此外,研究者根据血清Sclerostin水平将老年人分为两组,即高Sclerostin水平(Age-H)组和低Sclerostin水平(Age-L)组,发现Age-H组的认知功能评分和血清骨特异性碱性磷酸酶水平显著低于Age-L组。这一发现表明,高血清Sclerostin水平与老年人的骨代谢障碍和认知功能障碍相关。此外,研究者发现AD患者血清Sclerostin浓度与认知功能评分呈负相关,与血清Aβ水平呈正相关,并且血清Sclerostin水平高的AD患者认知功能评分显著低于血清Sclerostin水平低的AD患者,而血清Aβ水平相反。上述结果表明,血清Sclerostin水平与老年人和AD患者的认知障碍呈正相关,血清Sclerostin水平异常升高可能是认知能力下降的危险因素。
综上所述,该研究发现骨细胞源性Sclerostin可以通过血脑屏障抑制Wnt/β-catenin通路,加重衰老和阿尔兹海默症进展过程中的认知能力下降。该成果不仅揭示了骨脑轴代谢紊乱在阿尔兹海默症等疾病过程中认知功能损伤的机制,也丰富了器官之间相互调控的理论基础,为临床治疗阿尔兹海默症等神经退行性疾病提供新的思路。
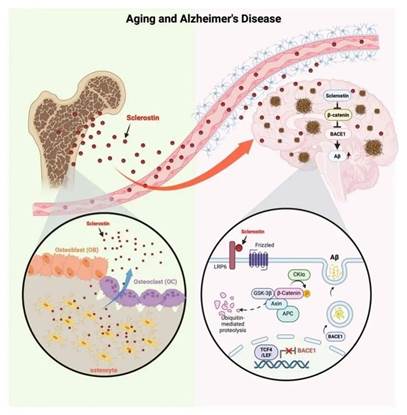
2024年2月26日,37000cm威尼斯医学院郭保生、蒋青及石云团队在Nature Metabolism在线发表题为“Osteocyte-derived sclerostin impairs cognitive function during ageing and Alzheimer’s disease progression”的研究成果,该研究发现在衰老和AD进展过程中,骨细胞分泌的硬化蛋白(Sclerostin, SOST)可以穿过老年小鼠的血脑屏障结合于神经元的LRP6受体,导致Wnt/β-catenin通路功能障碍,通过LRP6/β-catenin/β-secretase(BACE1)信号传导增加Aβ蛋白产生,从而加重认知功能损伤。37000cm威尼斯医学院郭保生教授、蒋青教授和石云教授为本文通讯作者;37000cm威尼斯医学院博士研究生石天舒、沈思虞和施勇为论文的共同第一作者。该研究获得国家自然科学基金重大项目、国家重点研发计划等各类项目支持。

专家点评
Lorenz Hofbauer(Technische Universität Dresden, Dresden, Germany)
This is an excellent paper that provides convincing experimental evidence for a role of osteocyte-derived sclerostin in neurodegeneration in several murine models and in people with Alzheimer’s disease, and it explores a therapeutic approach that is already available for severe osteoporosis. Overall, this is an exciting study that provides strong mechanistic links between osteocyte biology and neurodegeneration. This study may have wide implications regarding prevention or disease modulation of Alzheimer’s disease and similar age-related diseases. https://www.nature.com/articles/s42255-024-00990-4
(译文)这是一篇出色的论文,提供了令人信服的实验证据,阐明了骨细胞源性sclerostin蛋白在神经退行性疾病中的作用及其机制,证明用于治疗严重骨质疏松症的sclerostin中和抗体具有治疗阿尔茨海默症的潜能。总体而言,这是一项令人兴奋的研究,为骨细胞生物学与神经退行性疾病之间的强有力机制联系提供了支持。这项研究可能在阿尔茨海默症及类似衰老相关神经退化性疾病的预防或治疗方面具有广泛的影响。
原文链接:https://www.nature.com/articles/s42255-024-00989-x