由于缺乏足够的灵敏度和分辨率以及可靠的生物标志物,目前大约50%的癌症只有在晚期才被发现;目前临床可用的诊断成像方式,如计算机断层扫描(CT),磁共振成像(MRI)和正电子发射断层扫描(PET)等,其极限成像尺寸约为1毫米,而1毫米的微小病变就已经含有约105-106个肿瘤细胞。当肿瘤发生转移或者复发时,其恶性病变往往是极小的,目前临床的检测技术难以实现精准的检测。所以在早期准确地发现微小的恶性病变仍然是癌症诊断和治疗的一大挑战。
近期,化学化工学院蒋锡群教授课题组报道了一种可被酸性和乏氧循序激活的超灵敏磷光纳米探针Ir-D,用于癌症的早期检测。该纳米探针以对氧气敏感的具有深近红外发射磷光铱配合物为内核,通过酸敏感键连接水溶性高分子聚乙二醇为壳。聚乙二醇外壳不仅在循环过程中为纳米探针提供了稳定性和隐身功能,而且还可以作为酸性触发开关打开深近红外信号。利用对肿瘤微环境的酸性和乏氧的两步响应信号放大,结合深度近红外区的信号检测,该探针能够检测小鼠体内数百个肿瘤细胞或微米级的小原位肿瘤和转移灶。
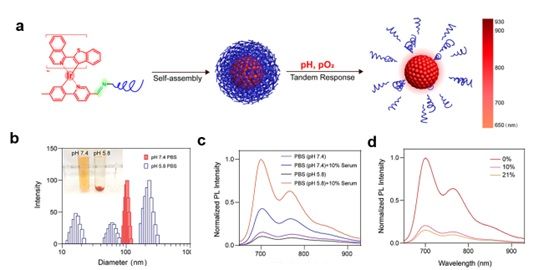
图1. Ir-D在不同pH和pO2条件下的形貌和光学性质表征。
在本研究中,作者首先研究了溶液中探针的酸触发的形貌的变化以及两步串联响应对于磷光信号的提升。结果显示在酸性条件下(如pH 5.8),随着时间的推移,纳米探针的形貌发生明显改变,由于酸敏感亚胺键的断裂,其聚乙二醇外壳会逐渐脱除,铱配合物疏水核会暴露出来并且发生聚集。从光谱表征来看,探针在703 nm处有最强的磷光发射峰,探针的信号在酸响应后的生理性溶液中发生约6倍的增强;与常氧条件下(21% O2)比,其酸响应后的溶液在乏氧状态下(0% O2)的信号增强了7倍。同时研究者还发现,合成的纳米探针在765 nm处具有一个肩峰,在深近红外(>800 nm)区域也具有明显的磷光发射,并且能够对酸和乏氧响应,该探针能够提供从近红外到深近红外的宽泛的成像窗口。
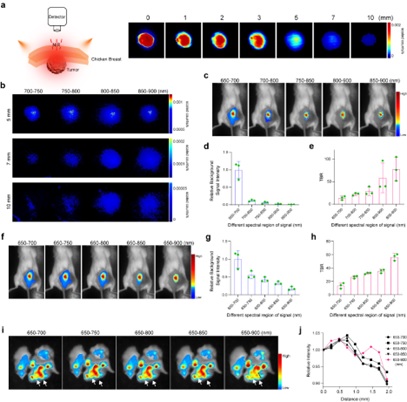
图2. 酸敏感纳米探针的细胞响应性成像和活体肿瘤特异性成像。
随后,如图2,作者研究了肿瘤细胞对探针的摄取以及探针在肿瘤细胞内的响应情况。结果显示,在pH 7.4时,将氧浓度从21%改变为1%,细胞中Ir-D探针信号显著增加;1%氧浓度时,降低pH会进一步增加磷光信号,Ir-D纳米探针具有pH特异性以及乏氧响应特性。进一步地,作者构建了多种类型的小鼠肿瘤模型验证了两步串联响应的探针对于肿瘤检测的特异性,Ir-D探针在多种皮下瘤、转移瘤以及PDX肿瘤模型中都能实现高灵敏度的成像。
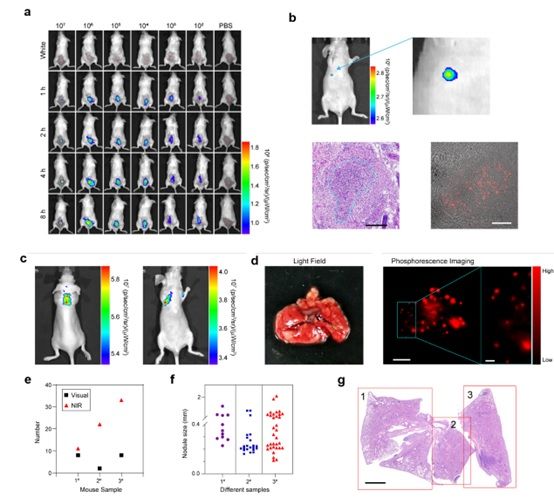
图3. Ir-D纳米探针对体内癌细胞、小肿瘤以及微小转移结节的检测。
作者通过皮下植入一定数量的H22癌细胞模型,进一步评估Ir-D的成像灵敏度。在小鼠背部植入不同数量的活H22细胞后,静脉注射Ir-D,并在预定时间点对小鼠进行成像。可以观察到,与注射PBS的小鼠相比,注射Ir-D的小鼠细胞在8 h时在该区域有明显的磷光信号。并且仅注射数百个癌细胞的小鼠的信号强度比PBS组平均高约2.0倍。此外,注射后8 h注射细胞区信号强度与注射细胞数相关。为了进一步评价Ir-D在检测早期微小肿瘤病变中的灵敏度,作者通过将肿瘤细胞类器官原位植入到小鼠乳腺中构建了早期肿瘤的动物模型。并在模型建立成功后,将Ir-D静脉注射到小鼠体内对动物进行成像。结果显示,植入微小肿瘤的乳腺部位具有明显的磷光成像信号。组织切片H&E染色证实癌细胞类器官位于乳腺内,大小为260×290 μm。冷冻切片的CLSM图像也显示,植入的类器官的区域有明显的探针信号。
此外,作者还构建了乳腺癌的肺转移模型来检验Ir-D探针的对于体内微小转移灶的检测能力。静脉注射Ir-D 探针24 h后,全身成像可以观察到小鼠肺部有明显的Ir-D的磷光信号。离体肺成像显示,注射Ir-D的磷光信号来源于肺转移结节。在多组小鼠样本中肉眼可分辨的结节只有2 ~ 8个,而Ir-D探针的磷光成像最多可检出33个结节。进一步测量发现,Ir-D探针检测到的肺转移结节的大小最大2.1 mm,最小115 μm。所有转移结节均通过H&E染色观察得到进一步证实,肺转移的总体诊断准确率在90%以上。
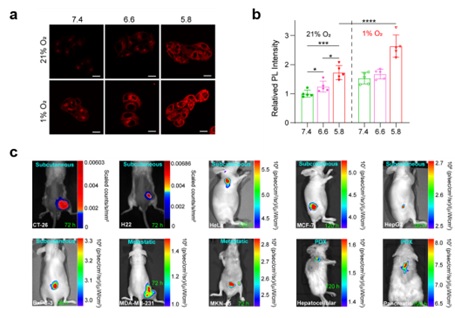
图4.体内外成像的对比度和穿透深度的提升研究。
最后,作者进一步评估Ir-D纳米探针的信号穿透性,富集Ir-D探针后的肿瘤离体成像表明Ir-D的光信号可以穿透7-10 mm的组织深度,并且在深近红外波段(800-850 nm和850-900 nm)的信号在深度组织(7-10 mm)成像时穿透性要明显高于近红外波段(700-750nm和750-800nm)。作者在利用Ir-D对荷瘤小鼠在不同波长发射区域进行全身成像时,观察到随着信号收集区域转移到深近红外区域,背景信号明显减少;同时,将信号收集波长增加到深近红外区时,信噪比显著升高。在对乳腺癌肺转移模型离体成像的结果进行分波段分析时发现,在650-900 nm检测范围内的肺转移病灶成像显示出最佳的对比度和分辨率。这些结果表明,所报道的深近红外探针通过将成像波长范围扩大到深近红外区域,可以显著提高乏氧成像的对比度。
此项研究工作充分发挥了深近红外光学检测灵敏度高、分辨率高等独特优势,阐明深近红外区域成像信号对于微小肿瘤成像质量的提升,扩展了两步串联信号放大策略在癌症早期检测中应用,为癌症早期检测提供了新思路。该工作以“Acid and hypoxia tandem-activatable deep near-infrared nanoprobe for two-step signal amplification and early detection of cancer”为题发表在《Advanced Materials》上。化学化工学院蒋锡群教授为论文通讯作者,博士生周森森论文为第一作者。工作得到了国家自然科学基金、国家重点研发计划以及江苏省自然科学基金的支持。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202212231